Los términos evaporación y ebullición suelen confundirse o usarse como si significaran lo mismo, pero no son iguales. Aquí te explicaremos qué diferencia hay entre evaporación y ebullición.
Rapidez
La evaporación es un proceso más lento y la ebullición es más rápida.
Temperatura requerida
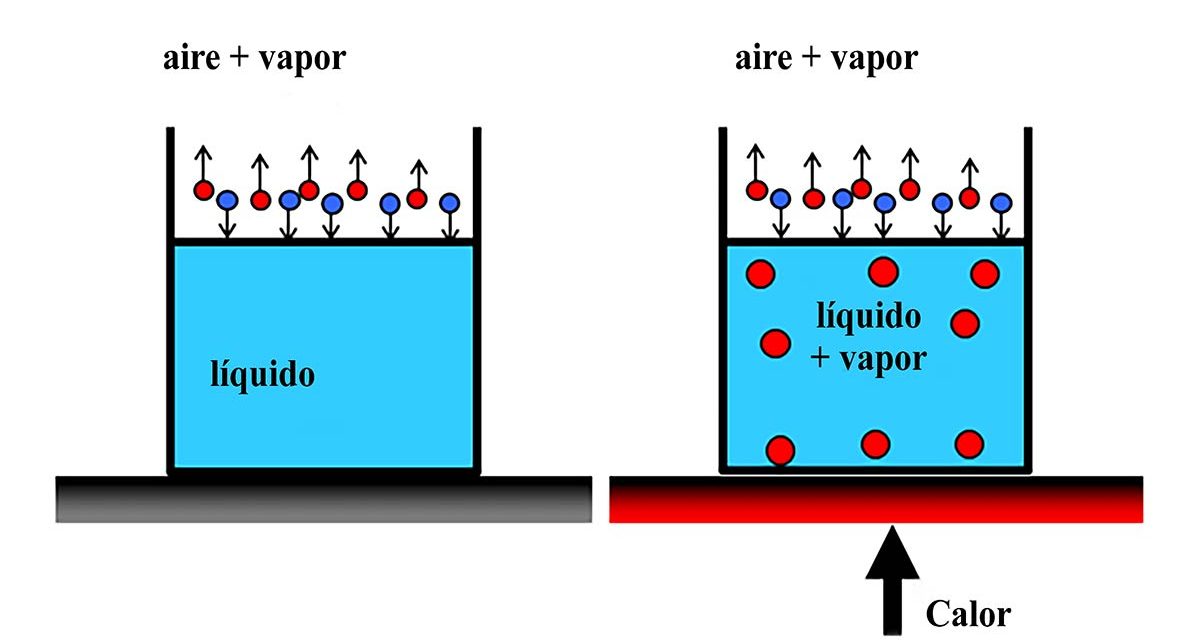
Un líquido se evaporará a cualquier temperatura por encima del punto de congelación. Si vertimos un poco de agua en el suelo a temperatura ambiente se evaporará lentamente. Si el agua estuviera más caliente, se evaporaría más rápido. Por el contrario, la ebullición ocurre sólo cuando el líquido alcanza una cierta temperatura, la cual llamamos punto de ebullición. El punto de ebullición del agua al nivel del mar es de 100 ° C (212 ° F).
Burbujas
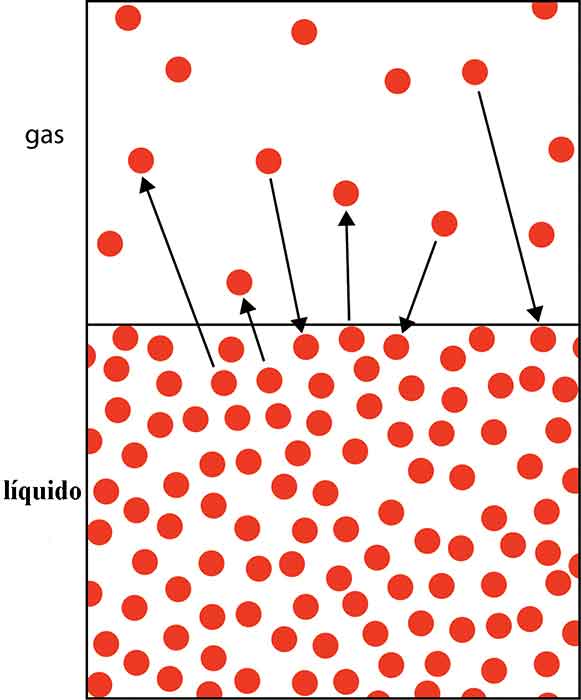
La evaporación no implica la formación de burbujas. Cuando un líquido se evapora, las moléculas individuales abandonan el líquido y pasan a formar parte del aire. En la imagen de abajo, los puntos representan moléculas. Las que dejan el líquido y pasan a formar parte del gas (aire) se están evaporando. Las que van de gas a líquido se están condensando. Cuando el agua en un vaso se está evaporando, las moléculas se mueven del agua al aire con más frecuencia que las del aire al agua. Así que hay una transferencia neta de moléculas de agua del líquido del vaso al aire. Como puedes ver en la imagen, este proceso no involucra burbujas. Por el contrario, cuando hierves agua, el líquido se convierte en gas con tanta rapidez que se forman burbujas de vapor de agua.
Ubicación del cambio a gas
Probablemente hayas notado que cuando calientas agua para que hierva, primero se forman burbujas en el fondo de la olla. Eso se debe a que, al principio, el fondo de la olla es el único lugar donde está lo suficientemente caliente como para calentar el agua hasta el punto de ebullición y convertirla en gas. Pero una vez que hierve, toda la olla de agua está en el punto de ebullición (100 ° C) y se forman burbujas en la mayor parte del agua. La evaporación, por otro lado, ocurre solo en la superficie del agua.
Fuente de energía
Para hervir un líquido normalmente requiere una fuente de energía externa, como el quemador debajo de la olla de agua en la que se están hirviendo unos huevos. La evaporación, sin embargo, usa la energía que ya está en el líquido. Si tienes un charco de agua, tienes algo de energía térmica, que generalmente proviene del medio ambiente. El calor en esa agua hace que algunas moléculas se muevan lo suficientemente rápido como para escapar al aire, es decir, evaporarse. No se requiere una fuente adicional de energía para la evaporación, y el agua no necesita alcanzar el punto de ebullición para evaporarse. Como hemos visto, el agua se evaporará a temperatura ambiente, es un proceso natural. El charco de agua o el agua en tu cabello cuando te acabas de bañar se evaporará sin que hagas nada en especial. Espera y se secará. Pero la ebullición no suele ocurrir de forma natural. Tenemos que calentar deliberadamente el líquido para que hierva.
Cambio de temperatura del líquido
Mientras el agua hierve, su temperatura permanece constante a 100 ° C. Una ebullición constante no hace que el agua esté más caliente que una ebullición media. Los huevos se cocinarán igual de rápido de cualquier manera. Por otro lado, la evaporación del agua enfriará el agua y cualquier superficie de la que se esté evaporando. Por eso cuando acabas de salir de la ducha sientes frío, es porque las moléculas de agua que se evaporan y se llevan calor de la piel. Esta es también la razón por la que transpiras en un día caluroso de verano. La humedad adicional en tu piel resulta en más evaporación, lo que enfría tu piel. Así que no te limpies el sudor de la frente; deja que se evapore solo para sentirte más fresco.
Factores que afectan la rapidez de la evaporación
Calor: La ropa que se seca en un tendedero se secará más rápido en un día de verano que en invierno.
Viento: Si sales de una piscina al aire libre cuando sopla el viento, sentirás frío porque el viento hace que el agua se evapore más rápido de tu piel, llevándose la energía térmica de tu piel más rápido, dejando tu piel más fría. Este efecto también es la causa del “factor de sensación térmica” del que se habla en los informes meteorológicos de los días fríos de invierno. No estabas en una piscina, pero tu piel siempre tiene algo de humedad. El viento hace que la humedad se evapore más rápido, llevándose más calor de la piel. Por eso es importante permanecer cubierto en los días fríos y con viento.
Humedad: El agua se evapora más rápido cuando el aire está seco. Cuando el aire está seco, hay menos moléculas de agua en el aire que regresan al líquido, por lo que el agua se evapora más rápido. Cuando el aire tiene muchas moléculas de agua (es decir, está húmedo), como en un día lluvioso, la evaporación es más lenta porque más moléculas de agua regresan al líquido.
Área de la superficie: El aumento de la superficie proporcionará más superficie desde la que se puede evaporar el agua. Por lo tanto, una toalla mojada se secará más rápido si se extiende en lugar de dejarla doblada o amontonada.